Los modelos de embriones humanos post-implantación son prometedores para desentrañar el desarrollo temprano
 Por Dr. Priyom Bose, Ph.D. Sep 12 2023 Revisado por Benedette Cuffari, M.Sc.
Por Dr. Priyom Bose, Ph.D. Sep 12 2023 Revisado por Benedette Cuffari, M.Sc.
Un reciente estudio de Nature evalúa el desarrollo postimplantacional en humanos utilizando modelos embrionarios basados en células madre embrionarias (CME) humanas naïve no modificadas genéticamente.
 Estudio: Modelos completos de embriones humanos de día 14 post-implantación a partir de células madre embrionarias ingenuas. Crédito de la imagen: Marko Aliaksandr / Shutterstock.com
Estudio: Modelos completos de embriones humanos de día 14 post-implantación a partir de células madre embrionarias ingenuas. Crédito de la imagen: Marko Aliaksandr / Shutterstock.com
Los modelos de células madre desvelan los secretos del desarrollo temprano del embrión humano
Los investigadores desarrollan un sistema de IA para ayudar a seleccionar mejor los embriones para la implantación
Antecedentes
Tras la implantación del embrión humano, una serie de acontecimientos como la morfogénesis de los tejidos extraembrionarios son esenciales para la gastrulación, el desarrollo futuro y la correcta organización de las células embrionarias.
Dado que durante esta fase se produce una elevada tasa de pérdida de embriones, es imprescindible comprender los acontecimientos asociados a la morfogénesis. Aunque esta información es crucial para comprender los problemas de fertilidad y los defectos del desarrollo, los estudios sobre este tema están asociados a retos tanto técnicos como éticos.
Es posible cultivar estructuras derivadas de blastocistos humanos; sin embargo, estos modelos no representan con exactitud los acontecimientos y la organización in vivo. Por lo tanto, es necesario desarrollar modelos de embriones derivados de células madre para estudiar las fases posteriores a la implantación.
Un modelo eficaz de embrión humano integrado post-implantación debe tener una presencia continua de equivalentes de células vitales, como trofoblastos, endodermo primitivo, mesodermo extraembrionario (ExEM) y células pluripotentes similares a epiblasto. Este modelo debe tener compartimentos embrionarios prominentes con una organización morfológica y estructural adecuada, así como poseer un disco embrionario adecuado, un disco bilaminar, un hipoblasto, una unidad amniótica polarizada, un saco vitelino polarizado, un compartimento similar al trofoblasto y una cavidad coriónica.
Las CME ingenuas de ratón se han utilizado para recapitular ex útero y estudiar las fases posteriores a la gestación. Se desarrollaron modelos sintéticos de embrión completo (SWEM) derivados de células madre, que pasaron a denominarse SEM, para estudiar la fase posterior a la implantación de embriones humanos.
Estudios anteriores han demostrado que las SEM de ratón pueden progresar dinámicamente más allá de la fase de gastrulación y alcanzar fases tempranas de organogénesis del desarrollo. Por lo tanto, las células pluripotentes ingenuas de ratón pueden utilizarse como fuente potencial de tejidos embrionarios y extraembrionarios para desarrollar modelos embrionarios "organogénicos".
Acerca del estudio
La disponibilidad de protocolos optimizados para que las células madre pluripotentes humanas (PSC) bidimensionales (2D) in vitro se diferencien en células maduras podría proporcionar una mejor comprensión de las vías transcripcionales, mecánicas y de señalización asociadas a la embriogénesis temprana.
Teniendo en cuenta los recientes progresos en las SEM de ratón y los avances en las condiciones de las células madre pluripotentes (PSC) humanas ingenuas, el presente estudio evaluó la posibilidad de utilizar estas células para desarrollar estructuras complejas similares a embriones peri/postimplantación que puedan progresar a estadios pre/peri-gastrulación ex útero.
Hallazgos del estudio
Utilizando el método descrito en un modelo de ratón, el presente estudio generó SEM postimplantación humanas autoorganizadas a partir de ESC ingenuas. A diferencia de los protocolos de derivación de MEB de ratón, el protocolo del presente estudio no requirió modificación genética ni sobreexpresión de factores de linaje exógenos para que las CME ingenuas se diferenciaran en linajes embrionarios clave esenciales para las etapas de desarrollo.
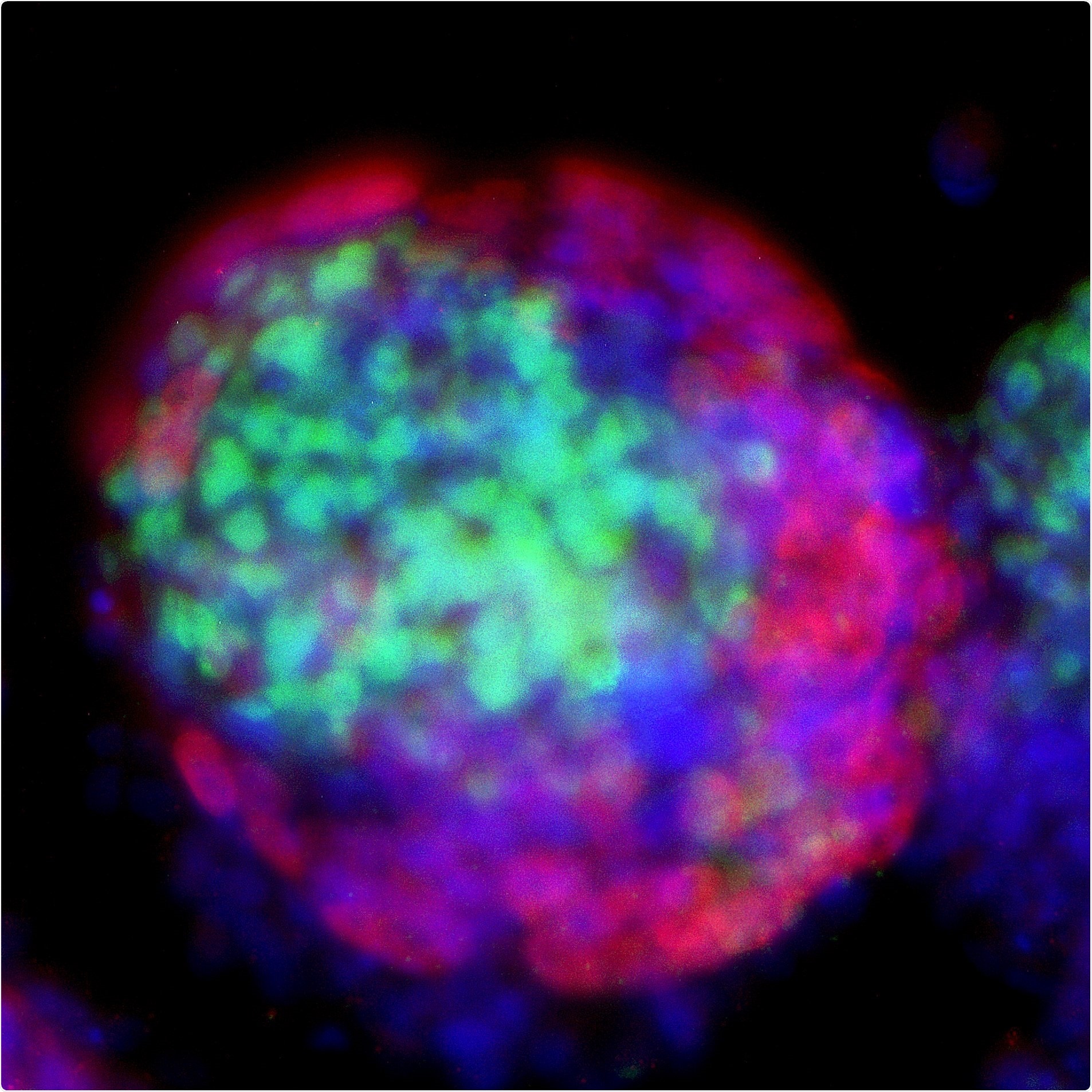
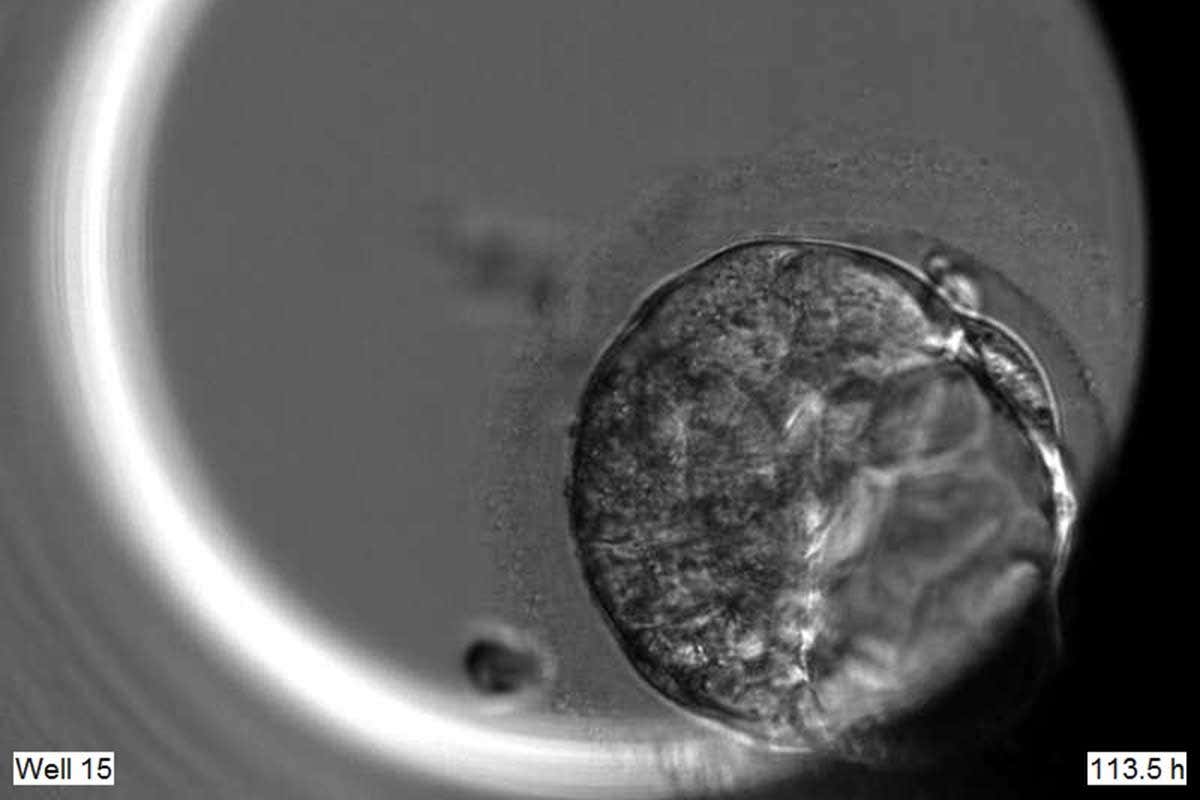
Se describió la capacidad de autoorganización de las PSC ingenuas para generar compartimentos embrionarios y extraembrionarios, incluido el ExEM. En particular, los SEM humanos ex útero recién creados se asemejaban a la arquitectura tridimensional (3D) y a los marcadores de desarrollo cruciales de los embriones humanos naturales in útero, en particular de 7-8dpf a 13-14dpf según los estadios Carnegie 5a-6a. Los estadios de Carnegie son un sistema estandarizado utilizado por los embriólogos para describir la madurez de los embriones.
Se observó una distribución espacial adecuada de los linajes celulares, en la que se formaron compartimentos embrionarios y extraembrionarios definidos en ausencia de fecundación o interacción con los tejidos maternos. Y lo que es más importante, esto se consiguió sin utilizar una vía de señalización externa dirigida para inducir la autoorganización de las células agregadas. Así pues, a nivel estructural, el SEM humano recién desarrollado se asemeja significativamente, aunque no es idéntico, a las condiciones naturales in utero.
El cuerpo embrionario (EB) generado no contenía los marcadores más básicos y definitorios de los modelos embrionarios integrados. Por ejemplo, los agregados tipo EB carecían de linajes celulares clave de los embriones en desarrollo, como el visceral, el linaje trofoblástico y el endodermo primitivo parietal.
Además, las EB carecían de disco embrionario, disco bilaminar, saco vitelino, hipoblasto y compartimento circundante similar al trofoblasto, que son características estructurales esenciales de los embriones en desarrollo. Los agregados similares a EB también tenían una capacidad limitada para progresar estructuralmente a las siguientes fases de desarrollo tras la formación inicial del agregado. Así pues, estos agregados EB no pueden considerarse modelos de embriones.
Conclusiones
Es importante estudiar el desarrollo postimplantacional humano temprano para comprender mejor la embriogénesis humana, lo que también proporcionará importantes conocimientos sobre la pérdida temprana del embarazo y el desarrollo de defectos congénitos. El objetivo del presente estudio era desarrollar un modelo embrionario que contuviera todas las estructuras embrionarias importantes, lo que ayudará a futuras investigaciones sobre la embriogénesis temprana.
Los agregados EB formados en este estudio no cumplían todos los criterios; por lo tanto, no puede utilizarse como modelo para estudiar el desarrollo embrionario. Teniendo en cuenta las estructuras embrionarias bien definidas desarrolladas en este estudio, es posible que, superando las limitaciones asociadas a la formación de agregados EB, este modelo pueda utilizarse para estudiar la embriogénesis temprana.